.,1,.Argentina,296,.Armas,39,.Asia - Pacifico,413,.Brasil,210,.Canada,39,.Chile,189,.Colombia,76,.Ecuador,50,.Guerra Antisubmarina (ASW),13,.Industria Naval,299,.Latinoamerica,306,.Malvinas / Falkland 1982,93,.Mujeres en Submarinos,49,.OTAN,275,.Peru,161,.Polonia,30,.Rusia,134,.Submarino Museo,87,.Tecnologia,205,.Tecnología Submarina,3,.Venezuela,26,"La caza del Octubre Rojo",1,##AlianzaAUKUS,1,##AtaquesGaza,1,##Atse,1,##Australia,1,##Becas,1,##Defensa,1,##FuerzaLaboral,1,##IndustriaDefensa,1,##Marina Real Canadiense,1,##SubmarinosClase214,1,##VentaAutorizada,1,#Acuerdos Bilaterales,1,#Alianza China-Pakistán,1,#Alianza Estratégica,1,#Alianzas de Defensa.,1,#Apoyo a Submarinos,1,#Armada China,1,#Armada de Chile,3,#Armada de los EE. UU.,1,#Armada de Pakistán,10,#Armada del Ecuador,1,#Armada Española,1,#Armada Francesa,2,#Armada India,1,#Armada Polaca,1,#Armada Sudafricana,1,#Ártico,1,#Astilleros Wuchang,1,#Ataque Simulado,1,#Base Naval,1,#Bloqueo,1,#Brest,1,#Capacidades operativas,1,#Clase 209/1400L,1,#Clase Barracuda,1,#Clase Borei,1,#Clase Delta IV,1,#Clase Kilo,1,#Clase Nimitz,1,#Clase Suffren,1,#Clase Walrus,1,#Clase Yasen,1,#Colaboración Industrial,1,#Comandante de la Zona Marítima Atlántica (CECLANT),1,#Comando de Operaciones Navales,1,#Combustible Nuclear,1,#Conflicto,1,#Construcción de submarinos.,1,#Construcción naval,1,#Cooperacion,1,#Cooperación en Defensa,1,#Cooperación Internacional,1,#Cooperación Militar,1,#Cooperación Naval,1,#Defensa,1,#Defensa Cooperativa,1,#Defensa Nacional,1,#Defensa Naval,3,#DefensaMutua,1,#Desarrollo,1,#Desplazamiento,1,#Diseño de Submarinos,2,#Disponibilidad en el mar,1,#Dominio submarino,1,#DRDO,2,#DronesSubmarinos,2,#Ejercicio Ibsamar,1,#Ejercicio OTAN 1999,1,#Ejercicio Subsar,1,#Ejercicios Navales,2,#Energía Nuclear,1,#Enfermera,1,#Entrenamiento,1,#Entrenamiento conjunto,1,#Estabilidad del buque,1,#Estrategia A2/AD,1,#Estrategia Naval,1,#Exocet,1,#Exportación,1,#Exportaciones,1,#Flota Híbrida,1,#Framatome,1,#Fuerza de Autodefensa Maritima Japonesa,1,#Fuerza submarina,1,#Guam,1,#Guerra Submarina,1,#GuerraSubmarina,1,#Hindustan Shipyard Limited,1,#HNLMS Walrus,1,#Howaldtswerke,1,#Huntington Ingalls Industries,1,#Hyundai Heavy Industries (HHI),1,#Île Longue,1,#Impresión 3D,1,#Indopacifico,1,#Inmersión,1,#Inmersión estática,1,#Integracion,1,#Inteligencia Artificial,1,#Interacción Marítima-2025,1,#Interoperabilidad,1,#Isaac Peral,1,#Le Vigilant,1,#LR,1,#Make in India.,1,#Marina Real Británica,1,#MBDA,1,#MDL,1,#Minirreactor Nuclear,1,#Ministerio de Defensa,1,#Misil Exocet,1,#Misiles,2,#Misiles Harpoon,1,#Modernización,2,#Modernización.,1,#ModernizacionDeSubmarinos,1,#MSubs,1,#Narciso Monturiol,1,#Pacifico Occidental,1,#PlataformasAutonomas,1,#Plymouth,1,#Propulsión AIP,1,#Propulsión Independiente del Aire (AIP),1,#Propulsion Nuclear,1,#Propulsión Nuclear,1,#Proyecto Scylla,1,#Pruebas en el Mar,1,#Recalificación,1,#Relaciones Internacionales,2,#Relaciones Marítimas.,1,#Safecap,1,#Seguridad Naval,1,#Sistema AIP,1,#Sistema de Propulsión AIP,1,#Sistemas Submarinos,1,#SkaramangasShipyards,1,#SNLE,1,#Soporte en Servicio,1,#STEM,57,#Submarinista,2,#Submarino Convencional,2,#Submarino KSS III,1,#Submarino S-80,1,#Submarinos,3,#Submarinos de Ataque,2,#Submarinos de ataque rápido,1,#Submarinos de Clase Isaac Peral.,1,#Submarinos de Clase S-80,1,#Submarinos de Propulsión Nuclear,1,#Submarinos Diésel,2,#Submarinos Furtivos,1,#Submarinos Nucleares,2,#SubmarinoToti,1,#Sudáfrica,1,#Tasa de disponibilidad,1,#Tecnología,1,#Tecnología Avanzada,1,#Tercera Zona Naval,1,#Terremoto,1,#Tipo 039B,1,#Tipo 096,1,#Tipo 212a,1,#Tipo Virginia,1,#Transferencia de Tecnología,1,#TransporteEspecial,1,#Tsunami,1,#UE,1,#VehiculosSubmarinosNoTripulados,1,#VelocidadSubmarina,1,#Vulnerabilidad de Bases.,1,#Vulnerabilidad Portaaviones,1,#WHOI,1,1:350,1,1ra Guerra Mundial,14,209/1100,1,209/1200,7,209/1400,8,214,1,218SG,1,2da Guerra Mundial,68,3D,1,636.3,1,667BDRM,2,Abastecimiento,1,Abel Basti,1,Abengoa,2,Abril,1,ABYSS,1,accidente submarino,142,Accidentes,2,Accidentes Navales,2,Acero para Submarinos,1,Actualidad,4,ACTUV,4,Acuerdos,3,Adaptado,1,ADCAP,2,Adelaida,1,ADEREX,1,ADESCAP-SB,2,Adiestramiento,85,Adiestramiento Naval,1,ADITAC,1,Adolf Hitler,1,adquisiciones,29,Adquisiciones.,1,AE1,1,Afirmacion de Pabellon,1,Africa,13,AGASM - Asociación submarinistas franceses,3,Aguas Someras,1,AIP,39,AIP.,1,Akula,1,Alanger,1,Alberto Guglielmotti,1,Alejandro Amendolara,1,Alemania,111,Alexander Nevsky,1,Alexandre Galante,1,Alianzas,1,alistamiento,1,Almanaque 2016,1,Almirante Merino" (BMS-42),3,Alseamar,1,Amas Submarinas,1,Amazul,2,AMRJ,5,Amur 1650,4,Analox,1,Angelo Nicolaci,1,Anil Jai Singh,1,Aniversa,1,Aniversario,49,AnnualEx,1,Antares,1,Anuncios,2,ARA Salta (S-1),4,ARA Salta (S-31),22,ARA San Juan (S-42),89,ARA San Luis,1,ARA San Luis (S-32),38,ARA Santa Cruz (S-41),17,ARA Santa Fe (S-11),4,ARA Santa Fe (S-21),24,ARA Santa Fe (S-3),4,ARA Santiago del Estero (S-12),4,ARA Santiago del Estero (S-2),4,ARA Santiago del Estero(S-22),7,Arabia Saudita,1,ARC Bolivar,1,ARC INdomable,13,ARC Intrepido,14,ARC Pijao,18,ARC Tayrona,14,ARCH SS-20 Thomson,21,ARCH SS-21 Simpson,26,ARCH SS-22 Carrera,24,ARCH SS-23 O´Higgins,28,Argelia,7,Arkhangelsk (K-562),1,Armada Argentina,10,Armada de Chile,2,Armada de Colombia,1,Armada de la India,1,Armada de la República de Corea (ROKN),1,Armada de Pakistán,1,Armada de Singapur (RSN),1,Armada de Turquía,1,Armada del Ejército Popular de Liberación,1,Armada Española,9,Armada Helénica,4,Armada India,2,Armada Popular de Vietnam,1,Armada Rusa,1,Armamento,18,armas submarinas,2,Armscor Dockyard,1,Arnaldo Funes,1,Arqueología Submarina,1,Arribos,2,Arsenal do Alfeite,1,Artico,6,Ártico,9,Articulos,63,ARV Caribe S-32,2,ARV Carite,1,ARV Carite S-11,4,ARV Picúa,1,ARV Sábalo S-31,1,ARV Tiburón (S12/S21),1,AS-12,1,AS-12 Losharik,2,ASC,2,ASC Pty Ltd,2,ASDIC,3,Aselan,1,Aselsan,1,Asia - Pacifico,13,ASMAR,5,ASMAR.,2,Asociación Submarinistas Alemanes - VDU,2,Asociación Colombiana de Submarinistas “ASOCOLSUBMA”,2,Asociación de Oficiales Submarinistas del Perú,1,Asociación Helénica de Submarinistas,1,Asociaciones,6,ASR-II,1,Astillero de Gölcük,1,Astillero Naval Golcuk,2,Astillero Naval Gölcük,2,Astillero SIMA,2,Astillero SIMA-PERU S.A.,8,Astilleros,11,Astilleros Sevmash,2,ASW,16,ASW.,1,ATech,1,Atlantic Coach 2015,1,Atlántico Sur,3,Atlas,1,ATLAS ELEKTRONIK,6,ATP-10,1,ATP-57,3,Augusto Conte de los Ríos,6,AUKUS,49,Australia,84,Autralia,4,AUV,7,AWS,16,B-276 Kostroma,1,B-39,1,B-586 Kronstadt,1,B-602 "Magadan",3,B-608 Mozhaisk,1,Babcock,2,BAE Huancavilca SS-102,14,BAE Shyri SS-101,31,BAE Systems,19,Bahia (S-12),3,bajas,4,Baltico,2,BALTOPS,1,Bandar Abbas,1,Bangladesh,2,Banquisa,1,BAP Angamos (SS-31),13,BAP Antofagasta (SS-32),8,BAP Aptao (SS-42),5,BAP Arica (SS-36),10,BAP Chipana (SS-34),11,BAP Dos de Mayo,1,BAP Ferré,2,BAP ISLAY (SS-35),6,BAP La Pedreira (S-49),2,BAP Pacocha (S-48),11,BAP Palacios,2,BAP Pisagua (SS-33),23,BAP San Lorenzo (ART-322),1,BAP Tiburón,1,Barracuda,1,Base de Submarinos,1,Base de Submarinos da Ilha da Madeira,1,Base de Submarinos Talcahuano,1,Base Naval Contralmirante Agustín Armario,1,Base Naval de Cartagena,2,Base Naval de Point Loma,1,Base Naval de Submarinos de la Isla de Madeira (BSIM),1,Base Naval Mar del Plata,6,Base Naval Talcahuano,2,Bases Navales,3,Batalla del Atlantico,2,Baterias,18,Baterias / Ion-Litio,22,Baterías de Iones de Litio,1,Baterías de Litio,3,Baterias para submarinos,5,bautismo,9,bautismo de fuego,2,BBC ONE,2,Belgica,1,Belgorod,4,bentos,3,Bester-1,4,Black Carillon,1,Black Shark,1,Block IV,1,BlueWhale,1,BNS Joyjatra,1,BNS Nabajatra,1,BNS Slava,2,BOE,1,BOGATUN,1,Bolsa de Fráncfort,1,Borei-A,2,Botadura,42,Brummel Vazquez,1,Buceo,1,Bulavá,7,Bulgaria,3,Buque de Apoyo Submarino,4,búsqueda y rescate,104,Buzos,1,Buzos tacticos,2,C-3,1,C-4,1,Cables Submarinos,1,Cabo de Hornos,1,Callisto,3,Cam Ranh,1,CAMNE,1,Canadá,13,Capacitación,1,Capacitaciones,22,CARI,1,Carlos Alberto Damelio,1,Carlos Damelio,1,Carlos Losana Perales,1,Carrier Strike Group 10,1,Cartagena,1,Cartago,9,Cartas,1,Cascos y Estructuras,19,Cassidian,1,Cavitación,1,CDB Rubin,1,CDR,1,CENTCOM,1,Ceremonia,10,ceremonias,131,certificación de una escotilla,1,Certificaciones,1,Ceuta,1,CFB Esquimalt,1,CFD,1,Chief,3,CHILEMAR,15,China,72,china Shipbuilding & Offshore International Company,1,Christian Alfredo Widmann,2,Christian D. Villanueva López,1,CIA,1,CIAMA,3,CienciayTecnologiaMilan,1,CINAR,3,Cine,9,Cine y Series,8,Clase Barracuda,3,Clase 0,1,Clase 035G,2,Clase 093,1,Clase 093G Shang,2,Clase 209NG,5,Clase 600,5,Clase A,1,Clase A17,1,Clase A26,17,Clase A26 Blekinge,7,Clase Agosta,3,Clase Agosta 90B,1,Clase Akula,8,Clase Alpha,1,Clase Arihant,2,Clase Astute,24,Clase Attack,1,Clase Balao,1,Clase Blekinge,1,Clase Borei,1,Clase Boréi,2,Clase Boréi-A,1,Clase Cetus,1,clase Challenger,1,Clase Chang Bogo - III,5,Clase Changbogo - III,4,Clase Collins,10,Clase Columbia,8,clase Daphne,1,Clase Dapnhé,5,Clase Delfin,1,Clase Delta IV,1,Clase Delta-IV,1,Clase DGK,1,Clase Dreadnought,3,Clase Echo,1,Clase Fateh,3,Clase Flota,1,Clase Foca,2,Clase Foxtrot,5,Clase Gato,2,Clase Ghadir,3,Clase Gotland,8,Clase Graney,1,Clase Guppy,1,Clase Gür,2,Clase Hangor,6,Clase Invincible,1,Clase Isaac Peral,3,Clase Jang Bogo II,1,Clase Jangbogo,2,Clase Jin,2,Clase Juliett,2,Clase Kalvari,14,Clase Kilo,13,Clase Kilo 636,1,Clase Kilo Mejorado,1,Clase Kobben,4,Clase KSS-III,3,Clase Lada,6,Clase Le Redoutable,1,Clase Los Angeles,13,Clase Los Ángeles,1,Clase Ohio,8,Clase Orca,1,Clase Orka,1,Clase Oscar-II,2,Clase Preveze,4,Clase Reis,6,Clase Riachuelo,8,Clase Romeo,1,Clase Romeo (Proyecto 633),2,Clase Rubis,2,Clase Ruby,3,Clase S-60,1,Clase S-70,4,Clase S-80,24,Clase S26T,5,Clase Salta,1,Clase Sauro,4,Clase Scorpene,1,Clase Scorpène,1,Clase Seawolf,6,Clase Shang,1,Clase Sierra,4,clase Södermanland,2,clase Son Won-il,1,Clase Soryu,14,Clase Sōryū,1,Clase SSN(X),1,Clase Suffren,6,Clase SX 506,1,Clase Taigei,11,Clase Tikuna,2,Clase Todaro,3,Clase Trafalgar,3,Clase Tridente,16,Clase Tupi,12,Clase Typhoon,13,Clase Ula,13,Clase Upholder,7,Clase Vanguard,4,Clase Varshavianka,5,Clase Victoria,16,Clase Victoria.,1,Clase Virginia,54,Clase Walrus.,10,Clase Whiskey / Proyecto 613,4,Clase Yankee,1,Clase Yasen M,2,Clase Yasen-M,3,Clase Yuan,5,Clase Yuan Tipo 039B,1,Clase Zhou,1,Cofs,6,Cohere,1,colaboración,1,Colaboración Estratégica,1,Cold Response,2,colisión,35,Comandante Azcueta,1,Comandante de Submarinos,23,Comando de la Fuerza de Submarinos.,21,Comandos Anfibios,2,Combate Naval,4,Comics,1,cómics,3,Comisionado,6,Compact Rapid Attack Weapon - CRAW,1,Complejo Naval de Itaguaí,1,COMPTUEX,2,Computadora de control Tiro,1,COMPUTEX,1,COMSUBNATO,3,COMSUBPAC,2,Comunicaciones,8,Comunicaciones Submarinas,1,Comunicados,1,Comunidad,1,condecoraciones,6,Conferencia de Submarinos de las Américas (SCOTA),3,Conferencias,13,Conflictos,2,Congresos,3,Conmemoración,1,Consola de Gobierno,3,Construcción de Submarinos,3,Contramedidas,3,contrato,1,Contratos,62,Control Averias,1,Control del Mar,1,CONVEMAR,1,Convertidores,1,Cooperación,4,Cooperación Internacional,1,cooperación naval,1,Coproducción de Submarinos,1,Corea del Norte,12,Corea del Sur,73,Corea del Sur.,1,Corte de Casco,1,Cosme Garcia,2,COSPAT,1,COTA 14,1,COVID-19,4,CPSP,9,Crisis,1,Crisis de los Misiles,1,Crocodile,1,Cronograma,1,CRRC,1,CSBC Corp,1,CSBC Corp.,2,CSBC Corporation Taiwan,2,CSS Hunley,2,CTBTO,2,Cuba,3,Cultura Naval,1,Curiosidades,2,curso,2,Curso Comandante de Submarinos,1,Curso escape,7,cursos,10,D-26 Bouchard DEBU,1,Daewo,2,Daewoo Shipbuilding & Marine Engineering Co,1,DAMEN,5,Daniel Prieto,8,DAPA,3,DAPHNE,2,DARPA,2,DARPA SUBOFF,1,Das Boat,1,Dassault Systemes,1,Dassault Systèmes,1,Datos Subs,7,David Claudio Lagar,4,David Marquet,1,DDS ( Dry Deck Shelter),1,de Defensa,1,De Grasse,1,decomisos,23,DeepBlue2022,1,Defensa,9,DEFENSA ANTIAEREA SUBMARINA,1,Defensa Antisubmarina,1,Defensa Asimétrica,1,Defensa Nacional,3,Defensa Naval,1,defensa y seguridad,2,Defensa.,1,Delfines,1,Delphinus Engineering,1,Delta IV,1,DeltaIV,2,Derecho del Mar,1,Desguace,7,Desguace Naval,1,Despliegues,80,destino final,17,Detección Acústica Submarina,4,detección subacua,4,Deutschen Marinemuseum,1,DEVELOGIC,1,DEYSEG,1,DGK,1,Dia D,1,Dia del Submarinista,1,Dianca,1,Diego Quevedo Carmona,7,Diesel Electric Submarine Initiative - DESI,75,Dimensión Submarina,1,Dinamarca,2,Dinámica de Fluidos Computacional,1,Dique Flotante,1,Dique Young,1,diques secos flotantes,1,Dirección de Innovación y Desarrollo (DINDES),1,Dirk Kempthorne,1,Discursos,1,diseño y desarrollo,10,DISSUB,71,distintivo,1,Disuasión,2,Disuasión estratégica,2,Disuasión Nuclear,2,Disuasión Nuclear.,1,DM2A5,1,Dmitri Donskoy,2,Documental,11,Dolphin,3,Dolphin II,7,Dosan Ahn Chang-ho,1,Dr Pablo Castro,25,Drass,8,DRDO,1,DRDO India,3,DRIX,1,Drones,18,Drones Submarinos,2,Drones.Tecnologia,1,DSIT Solutions,1,DSME,9,DSRV,4,DYMA26,1,Dynamic Manta,14,DYNAMIC MARINER,1,Dynamic Messenger,2,Dynamic Monarch,4,Dynamic Mongoose,10,ECA Group,5,Eckernförde,1,Ecuaciones de Lanchester,1,Educacion,3,Educación,3,efe-sep,1,Efemérides,8,Egipto,12,egresos,3,Ehime Maru,1,Ejercicio Artic Dolphin,1,Ejercicio de Disparo Marítimo,1,Ejercicio de escape,1,Ejercicio Nordic Response,1,Ejercicio Prasthan-25 (XPR-25),1,Ejercicio UNITAS,1,Ejercicio UNITAS 2025,2,Ejercicios,180,Ejercicios Navales,2,Ejercicios Navales.,1,Ejercicios Silent Shark,2,Elac Sonar GmbH,3,ELBIT SYSTEMS,2,Electricidad,2,Electronica,7,elSnorkel,16,Emblemas,2,Emden,1,Emeraude (S-604),1,Emergencia Médica,1,emergencia submarino,57,Emergencias Submarinas,1,En Astilleros,38,En eterna patrulla,3,Endeavor Manta,1,Energía Nuclear,2,enigma,3,Enrico Toti,2,entrega/incorporación,1,Entrenamiento,4,Entretenimiento,9,Entrevistas,19,Eric Genevelle,1,Erich Saumeth,1,Escape de Submarinos,15,ESCAPEX,2,Escenarios,1,Escolta,1,escotilla de rescate,2,Escuadrón de Submarinos,7,Escuela de Submarinos,80,España,183,Especialidades,15,Espionaje,1,Espionaje Industrial,1,Espionaje submarino,1,ESPS Tramontana,1,Estado del Arte,1,Estados Unidos,4,Estela Turbulenta,1,Estrategia,3,Estrategia marítima India,1,Estrategia Naval,7,Estrecho de Ormuz,3,Eterna patrulla,1,EURONAVAL,4,Euronaval 2014,1,Europa,11,Europa.,1,Eurydce (S644),1,Evacuación,1,eventos,28,Exail,2,Exibiciones,1,Exocet,3,Expociciones,4,EXPODEFENSA,1,Exponaval,7,Exportación,1,Exposiciones,1,F21,1,Fabricación Aditiva,1,Facundo Rovira,1,Falkland 1982,1,fallas,2,Fateh,3,Fede Supervielle,1,FEINDEF,1,Felinto Perry K11,1,Felix Artuso,7,Ferias y Exposiones,1,Fibra Óptica,1,Filipinas,5,Fincantieri,23,Firma Acústica,1,Firmas Acusticas,1,Flanq,1,Fleet-Type,1,Fleetex,1,Flota del Norte,3,Flota del Pacífico,2,Flota Rusa del Norte,4,Flota Rusa Del Pacífico,2,Flotilla de Submarinos,9,FNS Améthyste (S605),1,Force Recon,1,FORONAVAL,1,Foros,1,fotos,6,Foxtrot,3,Fragata Cochrane,1,Francia,85,FRANCISCO FERNÁNDEZ MATEOS,1,Francisco Guido Rossomando,10,Fraterno,3,FSB,1,Fuerza de Submarinos,40,Fuerza Submarina,1,fuerzanaval.com,1,Fuerzas especiales,7,fumar,2,G7a,1,Gabler,8,Gadzhiyevo.,1,Galatée (S 646),1,Gastops,1,Gazzana (S525),1,General Dynamics Electric Boat,23,Geopolitica,1,Geopolítica,7,Geopolítica Indo-Pacífico,2,Geopolítica Naval,5,Geopolítica.,5,Ghadir-955,1,Ghost Sharks,1,Gibraltad,2,Gibraltar,1,Giorgias,1,GNYK,1,Goiás - S15,1,Golfo de Persico,1,Golfo Pérsico,2,Gonzalo Salinas,1,Gorka L Martínez Mezo,8,GPS,1,Grecia,28,Griegos,1,Groenlandia,1,Groton,1,grupo electrógeno,1,Grytviken,3,Guanabara S 10,1,Guerra Antisubmarina,15,Guerra Antisubmarina (ASW),28,Guerra Antisubmarina (ASW).,1,Guerra Asimétrica,2,Guerra Civil,1,Guerra de Malvinas,1,Guerra Electronica,1,Guerra Electrónica,1,Guerra Fria,25,Guerra Fría,6,Guerra Híbrida,1,Guerra Indo-Paquistaní,1,Guerra Naval,1,Guerra Submarina,8,Guerra submarina moderna,1,Guilherme Poggio,3,Gunther Prien,2,H-3 Rucumilla,2,HABETaS®,1,habitabilidad,1,HAGENUK,1,Hai Kun (ss-711),7,Hai Kun (海鯤,1,Hai Kun (海鯤),1,Hakugei (SS 514),3,Hanwha Ocean,28,Hanwha Ocean Co. Ltd.,9,HD HHI,1,HD Hyundai Heavy Industries,10,HDS-2300,1,HDW,5,HDW CLASE 214NG,1,Héctor Galisteo Streeksoff,1,helices,5,Helicopteros,1,Helmuth Walter,2,Hensoldt,4,Heraldica,1,Héroes Navales,1,Hi-Line,1,hidroacústica,3,Hidrodinámica,1,HII,3,HII Newport News Shipbuilding,1,Himno,1,HIPOPÓTAMO,1,Historia,190,Historia Naval,4,HISutton,3,HMAS Collins,1,HMAS Dechaineux (SSG 76),1,HMAS Farncomb,2,HMAS Onslow,2,HMAS OTAMA,1,HMAS Sheean,2,HMAS Stirling,2,HMCS Chicoutimi,8,HMCS Corner Brook,3,HMCS Victoria,1,HMCS Windsor,5,HMS Agamemnon,3,HMS Ambush,4,HMS Anson,7,HMS Artful,2,HMS Astute,4,HMS Audacious,5,HMS Audacius,1,HMS Cachalot,1,HMS Conqueor,2,HMS Conqueror,7,HMS Courageous,1,HMS Dreadnought,2,HMS E5,1,HMS Halland,1,HMS King George VI,1,HMS M2,1,HMS Ocelot,1,HMS Onyx,5,HMS Osiris,2,HMS Regent,1,HMS Spartan,2,HMS Splendid,3,HMS Superb,1,HMS Swiftsure,1,HMS Talent,3,HMS Tarpoon,1,HMS Tireless,2,HMS Trenchant (S91),1,HMS Triumph,4,HMS Trooper,1,HMS Valiant,2,HMS Vanguard,5,HMS Vengeance,1,HMS Victorious,2,HMS VIgil,2,HNoMS Utstein,1,Hobby,2,Hoggar-032,1,HOISTEX,1,Homenajes,14,HonoresMilitares,1,Howaldtswerke (HDW),2,HQ-186 Da Nang,2,HQ-187 Ba Ria-Vung Tau,2,HS Katsonis (S-123),1,HS Matrozos (S-122),1,HS Papanikolis,1,HSwMS Gotland,3,HSwMS Södermanland,1,HSwMS Uppland,3,Huancavilca,2,Huludao,1,Huntington Ingalls Industries,3,HY-80,2,Hyatt (SS-23),2,HYDRA,1,Hyundai,1,I-400,3,I-52,1,IAI,1,IANTN / RITN,2,ICBM,1,ICE CAMP,1,ICEX,2,ICN - Itaguaí Construções Navais,100,IDAS,2,Impresión 3D,1,Impresoras 3D,1,Impresos,2,IN MEMORIAM,1,Incendio,8,incendio en submarino,6,incidentes,6,Incorporacion,29,Incorporación,36,Incorporaciones,13,India,107,Indian Navy,2,Indo-Pacifico,5,Indonesia,34,Indopacifico,1,Indopacífico,1,Indra,1,Industria de Defensa,2,Industria Italiana,1,Industria Naval,552,Infografias,11,Informe,8,Informes,5,Infraestructura,1,Ing Carlos E. Torres,7,Ing. Isaac Peral,8,Ingeniería Naval,2,Ingeniero Cesare Laurenti,1,Inglaterra,3,Innovación,1,Innovación Naval,1,INS Aridhaman,1,INS Arighat,1,INS ARIHANT,4,INS Dakkar Tz-77,1,INS Drakon,4,INS Kalvani,3,INS Kalvari,2,INS Khanderi,3,INS Kursura,1,INS RAHAV,1,Ins Sindhudhvaj,2,INS Sindhurakshak,3,INS Sindhuratna,2,INS Vagir,3,INS Vagsheer,2,INS Vela,4,Insignia,1,Intecs,1,Inteligencia,1,Inteligencia Articifial,1,Inteligencia Artificial,1,Inteligencia Artificial (IA),1,Inteligencia Naval.,1,Inteligencia Satelital,1,Intercambios,1,Intereses Marítimos,3,International Submariners Congress,1,Interoperabilidad,1,Interoperabilidad OTAN,1,Investigación de Operaciones,1,Investigación y Desarrollo,46,Ion-Litio,4,Iones de Litio,1,IPMS Mar del Plata,1,Iran,11,Irán,4,Irlanda,1,IROV,1,ISA,3,Isaac Peral,1,ISC,1,ISMERLO,16,ISR,1,ISR Marítimo (Inteligencia,1,Israel,16,Itaguaí,6,Italia,78,ITS Scire,2,IXblue,2,Jabárovsk,1,Jangbogo II,2,Jangbogo III,6,Japon,51,Japón,4,Javier Navia,2,Javier Pery Paredes,1,JCET (Joint Combined Exchange Training),1,JFD-James Fisher,3,Jingei SS-515,1,JL-2,1,JMSDF,3,Jorge A Ricaldoni,1,Jorge Pereira,1,José Javier GUERRERO DEL CAMPO,7,José María Ramírez Iglesias,1,JS Chogei,1,Juan Carlos Federico Blume Othon,3,Juan Oliver Lorente,13,juegos,7,Juliett,1,Juliett 484,1,K 219,1,K-141 KURSK,11,K-18 Karelia,1,K-19,4,K-266,1,K-27,2,k-276 Kostromá,1,K-278 Komsomolets,2,K-278 Komsomolets,2,K-3,1,K-322 Kashalot,1,K-441,1,K-561 Kazan,1,K-562Arkhangelsk,1,K-564 Arkhangelsk,1,K184,1,Ka-27,1,Kaiten,1,Kalveri,1,Kambala,1,Kamchatka,1,Karl Dönitz,1,Karl Flach,5,Kawasaki Heavy Industries.Industria Naval,1,Kawasaki Shipbuilding Corporation,1,Kazan,2,Kazan (K-561),1,KIEL,7,Kilo,14,Kniaz Pozharski,1,kockum,3,Kockums,2,Kólpino,1,Kongsberg,3,KONGSBERG DEFENSE & AEROSPACE,1,Kongsberg.Kongsberg,1,Krasnodar,3,KRI 404 Ardadedali,1,KRI Alugoro (405),2,KRI Alugoro-405,1,KRI Cakra-401,1,KRI Nanggala 402,9,Kriegsmarine,2,Kronshtadt,2,KSS-II,4,KSS-III,11,KTA Naval System,1,KTA Naval Systems,2,L'Invincible,1,L3harris,3,LAAD,1,Labgene,2,Lada,4,Lanzamiento de Misiles,1,Lanzamientos,10,Lanzamientos de Torpedos,3,Larsen and Toubro (L&T),2,Laser,2,Latinoamerica,768,Le Foudroyant.,1,Le Minerve (S-647),3,Le Terrible,1,Le Tonnant,1,Le Vigilant (S618),1,Leonardo SpA,6,Lewis Mejía Prada,11,liam nisson,1,Liborio Palombella,1,Libros,8,Lic Bakic Guillermo,5,Licitaciones,5,Liderazgo,1,Litoral Argentino,1,Lockheed Martin.,5,Logística Naval,1,Los Flota,1,Lost 52 Project.,1,LR5,3,Lubeck,1,Luis Enrique Velez Roman,3,Luiz Padilha,1,LUUV,2,Magellan Aerospace,1,magnetohidrodinamica,2,Malasia,3,MAN Energy Solution,1,Maniobras,2,manteniemiento,6,mantenimiento,30,Mantenimiento Naval,5,Mantenimiento Submarino,2,Manual de Operaciones,1,Mar Arábigo,2,Mar Báltico,3,Mar de Barents,3,Mar de Japón,1,Mar de la China Meridional,1,Mar de Noruega,1,Mar del Norte,1,Mar del Plata,1,Mar Mediterraneo,2,Mar Mediterráneo,2,mar negro,5,Maratón,1,Marcelo Malara,1,MARCOM,1,Maria Petkovic,1,Mariano Sciaroni,22,MARICOSOM,1,Marina de Guerra del Perú,8,Marina Francesa,1,Marina Militare,4,Marina Real Canadiense,2,Marina Real de Malasia,1,marineschepen.nl,1,Marinha do Brasil,4,Marinha Portuguesa,2,Marmen,1,Marruecos,5,Martín Piazza,1,MASSEVEX,1,Master Chief,1,mastiles y antenas,7,Mazagon Dock,1,Mazagon Dock Shipbuilders,1,Mazagon Dock Shipbuilders Limited,1,Mazagon Dock Shipbuilders Limited (MDL),12,Mazagon Docks Ltd,2,MBDA,2,MEDEVAC,1,Medicina Hiperbarica,1,Medio Oriente,4,Mediterraneo,6,Mediterráneo,1,Mediterráneo.,1,memorando,1,memorando de entendimiento,1,MESMA,2,Methanol,1,Mexico,2,MH-60R Seahawk,1,midget,1,Minas,1,Mini Submarinos,9,Ministro de Defensa,2,minisubmarino ruso AS-28,1,Misil,3,Misil Antibuque P-700 Granit,1,Misil Harpoon,1,Misil K-4,1,Misil Oniks,1,Misil SM39,3,Misil SM40 Exocet,1,Misil Tomahawk,1,Misil Trident II D5,1,Misil YJ-19,1,Misiles,12,Misiles Balísticos,1,Misiles de Crucero,1,Misiles Kalibr,3,Misiles MdCN,1,Misiles Sineva,1,Mistral,1,Mitsubishi,1,Mitsubishi Heavy Industries Kobe,3,MK_54,1,MK-10 Submarine Escape and Immersion Equipment (SEIE),2,MK-11 Submarine Escape and Immersion Equipment (SEIE),1,MK-48,2,MK39 EMATT,1,MLU,6,MLU (Mid-Life Upgrade),1,MO-103,1,Modelado 3D,1,Modelismo,1,Modelismo cratch,1,Modelismo Kits,4,Modelismo Papel,1,Modernizacion,17,Modernización Naval,1,Modernización.,3,Monumentos,3,MOOG Australia,1,Motor Eléctrico de Propulsión (MEP),3,Motores para Submarinos,8,MRO,1,MTU,7,MU90,1,Mujeres en submarinos,6,Mundial.,1,Muratreis,1,Murcia,1,Musa,1,Museo de Submarinos,1,Museo Technik,1,Myanmar,1,Nanotecnologia,2,Narciso Monturiol,1,Narval S-631,1,NATO Submarine Rescue System (NSRS),1,Naufragios,3,nautilus,1,Naval Force,2,Naval Group,11,Naval Group (DCNS),112,Naval Submarine School,1,Naval Submarine School (NSS),1,Navantia,50,Nave Nodriza,1,navegacion,1,Navegación,1,Nedinsco,1,negocios,1,Nerpa,1,Nevesbu,2,Newport News Shipbuilding,7,NICOMEDES SANTA CRUZ,1,Niteroi,1,NORSUB-5,1,Northrop Grumman,1,Noruega,47,noticia,4,noticias,14,Novorossiysk,1,Novorossiysk (B-261),5,Novosibirsk,1,NRP Arpao (S161),21,NRP ESPADARTE,1,NRP Tridente,3,NRP Tridente (S160),15,NSS Guillobel,1,Nuclep,2,Nulcep,1,O´Brien (SS-22),2,Oberon,1,Obnisk,1,OCCAR,9,Ocean Infinity,3,Oceania,2,Oceano (S-118),1,Océano Índico,4,Ocio,42,Octubre Rojo,1,Offset,1,Ofrecimientos,2,OMI,1,Ontario.,1,OpenDays,1,Operación "Brilliant Shield",8,OPERACIÓN “HOKEHAMTON”,1,Operación ARCTIC,1,Operación Armonía del Mar Negro,1,Operación Awless,1,Operacion Baldur,1,Operación Banner,1,Operación de Fiscalización Marítima,3,Operación Grenada,1,Operación LATITUDE,1,Operacion MAr Abierto,3,Operación Neptuno,1,Operación Noble Shield,6,Operación Relentless,1,Operación Sea Guardian,11,Operación Sindoor,1,Operación Torch,1,Operaciones,14,Operaciones de Rescate,1,Operaciones de combate,5,Operaciones de Inteligencia,5,Operaciones de vigilancia,6,Operaciones Especiales,6,Operaciones Submarinas,8,Operaracion Irini,6,operativo,1,Opinión,19,Opiñión,1,OptiArray,1,Optics11,1,Optronico,8,ORCCA,1,Orel K-266,1,Organismos,1,Oriente Medio.,1,ORION,1,ORP Bielik,1,ORP Kondor,1,ORP Sęp,1,ORP Sokol,2,Orzeł,2,Osborne,1,Oscar,2,Oscar Daniel Siano,1,Oscar Filippi,1,OSI Maritime Systems,2,OTACV-S80,1,OTAN,526,Otto Kretschmer,1,Ouarsenis-031,1,p,2,P-3 Orion,2,P-75I,1,P-8A Poseidon,2,Pablo Javier Melara,3,Paises Bajos,41,Pakistán,15,Panama,1,Pandemia,6,Panorama,157,PASSEX,1,Patrulla de Guerra,1,Pearl Harbor,1,pecio,5,pecios,23,Percy Isaac Suárez Cáceres,2,Periscopio,12,Periscopio SERO 250,1,Periscopios,1,Perseo Techworks,1,Personal Militar,1,Peter Mulvany,1,Phoenix Dragon (511),1,Pietro Venuti (S 528),1,PIlas de Combustibles,1,Pirireis (S 330),4,Plan genesis,1,Plan Procyon,1,Playbook Merlin,1,Plazos de Entrega,1,Pluviôse,1,PNR Barracuda (S164),1,PNS Ghazi,1,PNS Hangor (S131),2,PNS/M KHALID (S-137),1,Poder naval Océano Índico,1,PoderNaval,2,Podmoskovie,1,Polonia,1,POLYPHEM,1,Portsmouth Naval Shipyard,1,Portugal,48,POSYDON,1,Precursores,20,Presentaciones,4,Presupuesto Militar,3,primera inmersión,1,Programa "Orka",3,Programa de Submarinos,1,Programa IDS,1,Programa Orka,3,Programa S-80,1,Programas,1,Propulsion,29,Propulsion AIP,29,Propulsión AIP,3,Propulsión Diésel,1,Propulsion Nuclear,6,Propulsión Nuclear,2,PROSUB,88,Proyecto,1,Proyecto 611,1,Proyecto 09852,2,Proyecto 636,9,Proyecto 636.1,3,Proyecto 636.3,17,Proyecto 667,2,Proyecto 667BDR,2,Proyecto 667BDRM,1,proyecto 671RTMK,1,Proyecto 677,2,Proyecto 677M,1,Proyecto 75,3,Proyecto 75 India,1,Proyecto 75I,16,Proyecto 885M Yasem-M,6,Proyecto 941,2,Proyecto 949,1,Proyecto 949A,1,proyecto 955 Borei,13,proyecto 955a Borei-a,2,Proyecto 971,2,Proyecto Cabot,1,Proyecto MILDEN,3,Proyecto Sphyda,1,Proyecto Yasen-M,2,Proyectos,6,Pruebas de fabrica,2,pruebas de inmersión,3,pruebas de mar,49,Pruebas de Puerto,2,PT Pal,1,PT PAL Indonesia,1,Publicaciones,6,Publicidades con submarinos,1,Puget Sound Naval Shipyard,1,Pump-jet,1,Punta Arenas,1,Qatar,1,QinetiQ,1,Quebec,2,R-29,1,radiacion,1,Radioecología,1,Rafael,1,Raigei SS-516,1,Raytheon,2,Reactores Nucleares,2,Reclutamiento,4,Reducción de Ruido,1,Regia Marina,1,Regreso,3,Regreso a Casa,1,Regreso a puerto,6,Reino Unido,40,Reino Unido.,3,Relato,4,Relato de Guerra,7,Relatos,1,Relevo de Comando,1,REMUS 600,1,Remus 620,1,Remus UUV,1,Renovación,9,reparaciones,6,Reparaciones Media Vida,27,REPMUS,1,Reportajes,2,Rescate Naval,1,rescate submarino,14,Reserva Naval,1,retiro,1,Retrasos Proyecto,1,Reunion,4,Revista de Marina.cl,1,Revista de Marina.es,1,Revista Fortín,2,Revista Naval,4,Revista Vigía,1,Revistas,2,Ricardo Burzaco,1,RIMPAC,8,RIMPAC 2026,1,Rio Grande do Sul (S-11),2,Rio III,1,ROASW,2,Roberto Marcelo Paz,24,Rodríguez Labandera,2,Roger L. Cotrina Alvarado,1,ROK Dosan Ahn Chang-Ho,1,ROKS Ahn Mu (SSB-085),3,ROKS An Jung-geun,1,ROKS Cheonan,1,ROKS Dosan Ahn Chang-ho,1,ROKS Dosan Ahn Chang-ho (SS-083),1,ROKS Dosan Ahn Changho (SS-083),1,ROKS SINDOLSEOK (SS 082),1,Rolls-Royce,1,Rolls-Royce-MTU,3,Rosoboronexport,1,ROV,2,Roy Wood,1,Royal Canadian Navy,4,Royal Canadian Navy (RCN),1,Royal IHC,2,Royal Navy,86,RSS Chieftain,1,RSS Conqueror,1,RSS Impeccable,3,RSS Inimitable,1,RSS Invincible,2,Rubin,1,Rumania,4,Rusia,114,RWUAS,1,S-10,1,S-1000,4,S-110 Glavkos,2,S-178,1,S-20 Humaita,1,S-21 Tonelero,1,S-353 PREVEZE,1,S-354 SAKARYA,1,S-355 18 MART,1,S-356 ANAFARTALAR,1,S-40,1,S-41 Humaitá,17,S-43,2,S-61 Delfin,2,S-62 tonina,4,S-71,1,S-71 Galerna,8,S-72 Siroco,1,S-73 Mistral,8,S-74 Tramontana,9,S-80,35,S-80Plus,5,S-81,1,S-81 Isaac Peral,26,S-82 Narciso Monturiol,1,S-83 Cosme García,2,S-84 Mateo García de los Reyes,1,S.A. (AASA),1,S101 SAS Manthatisi,4,S102 Charlotte Maxeke,2,S161 BNS Nabajatra,1,S162 BNS Joy Jatra,1,S20,1,S30 Tupi,6,S31 Tamoio,5,S32 Timbira,10,S33 Tapajo,9,S34 Tikuna,13,S42 (864),1,S529 Romeo Romei,4,Saab,29,SAAB -DAMEN,6,Saab Kockums,2,Sábalo(S-31),4,SACOR Siderotécnica SA,1,SAES,23,Safran Group,2,Sala de Maquinas,1,Salud,1,salvamento,9,Salvatore Todaro,2,San Diego,1,Santiago Aversa,1,Sanya,1,Saphir,1,SAR,7,SARMISS,2,SARSAT,1,SARSUB,15,SAS S99 ASSEGAAI ex-Johanna van der Merwe,3,satelite,1,Saukko,1,SBR-1 Riachuelo S-40,33,SBR-2,1,SBR-3 S42Tonelero,12,SBR-3 Tonelero,1,SBR-4 Angostura (S-43),5,scapa flow,2,Scire,1,Scorpene,25,Scratch,1,SDV,1,Sea Ceptor,1,Sea Dragon (793),1,SEA1000,1,Seabed Contructor,2,sebastopol,1,Segunda Guerra Mundial,2,Seguridad,2,Seguridad Báltica,1,Seguridad Internacional,1,Seguridad Nacional,1,Seguridad Naval,2,Sekiryu SS-508,1,Seminarios,1,sener,2,Sensores,6,SenToku,1,Ser Submarinista,217,Serie 60,1,Serie Perla,1,Serie S-70,1,Series TV,1,SERO 400,2,Servicio Activo,2,Shackleton 2014. S/Y Polonus,1,Shiplift,1,Shkval,2,Shortfin Barracuda,5,SIA Conferences,1,Siemens,2,SIFOREX,2,Sigilo,1,Sigilo Acústico,1,Silent Hunter,1,SIMA,5,SIMA Perú,1,Simulación de Monte Carlo,1,Simulacro de Escape y Rescate,1,Simuladores,11,Simuladores de Submarinos,8,Simuladores PC,3,SIMULIA PowerFLOW,1,Sinergia 25,1,Singapur,17,SINKEX,2,Sistema de Combate,1,Sistema de Gestión de Combate,5,Sistema de Mástil Modular Multifunción,1,Sistema de Navegación Táctica en Inmersión,1,Sistemas de Aire Respirable,1,sistemas de armas,2,Sistemas de combate,12,Sistemas de Gobierno,2,Sistemas de Navegación,6,Sistemas de Propulsión,18,SITDEF- PERU,2,Skaramangas,1,SLBM,2,SM U118,1,Smer,2,SMEREX,3,SMEREX 2025,2,SMERWG,3,SMG Cappellini,3,smg macallé,5,SMG Scire,2,SMX-26,1,SN-BR Álvaro Alberto,1,SNA,1,SNA Améthyste,1,SNA Casabianca,2,SNA Duguay-Trouin,2,SNA Perle,5,SNA Rubis,2,SNA Ruby,1,SNA Saphir,1,SNA Tourville,4,SNB Alvaro Alberto,16,SNLE,4,SNMG-1,1,SNMG1,1,SNMG2,2,snorkel,3,Sōgei,1,Sonar,48,sonar pasivo,1,Sonar Samdis 600,1,sonares,6,SRC,1,SRDRS,2,Sri lanka,1,SRV,3,SS 078 Yu Gwan-sun,2,SS Simpson,1,SS Thomson,1,SS Thomson S-22,1,SS-20 Thomson,1,SS-508 Sekiryu,1,SS-510 Shoryu,1,SS-517 Chougei,1,SS-711),1,SS-791 Hai Shi,1,SS-792 Hai Pao,1,SS-794 Hai Hu,1,SSBN,13,SSBN 3G,2,SSBN James Madison,1,SSBN L Inflexible S615,1,SSBN Project 667AU K-219,1,SSBN Tipo 094,3,SSGN,1,SSK,3,SSK SS-511 Oryu,1,SSN,9,SSN 764,1,SSN 780,1,SSN 787,1,SSN 796,1,SSN Suffren,1,SSN-791 Delaware,1,SSN-792 Vermont,1,SSN-AUKUS,7,Stari Oskol,1,STEM,3,STIRLING,3,STM,8,STN Atlas Elektronik,2,SUBCOMP,1,SUBCON,8,subdiex,26,SUBDIEX 2025,2,SUBEX,1,Submairno B-5,1,Submarine Rescue Diving and Recompression System,1,Submarine Rescue Vehicle,1,Submarine Training Facility San Diego,1,submariner memorial,2,Submarinista,1,Submarinista por un dia,1,submarinistas,1,Submarino,15,Submarino "B-380",1,Submarino B-67,1,Submarino C-4,2,Submarino Ceará,1,Submarino Clase Dosan An Chang-Ho,1,submarino compacto,1,submarino convencional,1,Submarino de Ataque,3,Submarino de ataque rápido,1,Submarino de Misiles Balisticos,2,submarino de misiles balísticos,1,Submarino DGK,1,Submarino Diesel,61,Submarino Ferré,1,Submarino M-256,1,Submarino Museo Griego "Proteus" (S-113),1,Submarino Museo O'Brien,9,Submarino n,1,Submarino No Tripulado,1,Submarino Nº361,1,Submarino Nuclear,256,submarino nuclear B-448 Tambov,1,Submarino Nuclear de Ataque,2,Submarino O13,1,Submarino Perdio,1,submarino peruano,1,Submarino ruso,1,submarino siniestrado,1,Submarino Sovietico,2,Submarino SSBN,6,Submarino TCG Batıray (S-349),2,Submarino Timbira,1,Submarino Tipo 212CD,3,Submarino Tipo Kilo,10,Submarino Tonina (S-62),1,Submarino Toro,1,Submarino U212NFS,10,Submarinos,43,Submarinos Dolphin,1,Submarinos Autónomos,1,Submarinos Clase 209/1400L,4,Submarinos Clase H,1,Submarinos Clase Hangor,1,Submarinos Clase Ohio,3,Submarinos Compactos,2,Submarinos Convencionales,80,Submarinos de ataque,5,Submarinos de ataque nuclear (SSN),2,Submarinos de ataque rápido,1,Submarinos de Bolsillo,1,Submarinos de Clase Virginia,2,Submarinos de Exportación,1,Submarinos de propulsión nuclear,1,Submarinos Diesel,103,Submarinos Diesel TKMS,5,Submarinos Eléctricos,1,submarinos en operaciones.,1,Submarinos enanos,4,Submarinos Expeditionary C-71,1,Submarinos Hundidos,78,Submarinos Midget,1,submarinos nucleares,32,Submarinos R/C,14,Submarinos Rusos,55,Submarinos Scorpene,2,Submarinos Tipo 214,2,Submarinos X-Craft,1,SubmarinosTrident,1,SubmarinoTCG 1. Inönü,1,Suboficial,1,SUBP-SS (Rt) JORGE ECHEVERRIA M,2,Subs en Guerra,50,SUBSAFE,1,SUBSAR,7,SUBTICS,1,Sudafrica,11,suecia,35,Sumergible F1,1,Supercavitacion,2,Survitec,1,Swimmer Delivery Vehicle,1,Sydney Sonartech Atlas,1,TACC,1,Tactico-Operativo,1,Tailandia,12,Taiwan,23,Taiwán,1,Tandanor,3,Tarantinos,4,TCG Anafartalar,1,TCG Anafartalar (S356),1,TCG Dumlupinar (D-6),1,TCG GUR,1,TCG Hizir Reis,2,TCG Uluçalireis,1,Tebaldo RICALDONI,2,Tecnologia,168,Tecnología,5,Tecnología Naval,4,Tecnología Submarina,1,Thales,5,THE PERISHER,12,ThyseenKrupp,23,ThyssenKrupp Marine Systems,49,Tipo 035G Ming III,1,Tipo 039A,2,Tipo 039B,2,Tipo 041,3,Tipo 094,1,Tipo 095,1,Tipo 206,19,Tipo 209,69,Tipo 209/1100,3,Tipo 209/1200,3,Tipo 209/1400,9,Tipo 209P,8,Tipo 209PN,1,Tipo 210,1,Tipo 212,15,Tipo 212 NFS,1,Tipo 212A,2,Tipo 212CD,5,Tipo 214,30,Tipo 214 NG,1,Tipo 214 TN,1,Tipo 218SG,10,Tipo A26,1,Tipo Balao,8,Tipo Barracuda,4,Tipo Cavallini,3,Tipo Guppy,16,Tipo Holland,2,Tipo KSS-III,11,Tipo Oberon,47,Tipo S26T,4,Tipo Scorpene,65,Tipo Scorpéne Evolved,2,Tipo STM500,2,Tipo VIIB,1,Tipo098,1,Tipos de Submarinos,1,TITAN,1,Titanic,2,TK-208 Dmitry Donskoy,4,TKMS,63,TNI AL,1,Tomahawk,1,Tomas Ramiro Pérez Romero,3,Tonina,1,Torpedo 47,1,Torpedo 62/ 2000),1,Torpedo Black Shark,4,Torpedo DM2 A4,2,Torpedo F21,3,Torpedo Mark 48,1,Torpedo Poseidón,4,Torpedo Spearfish.,1,Torpedo Spearfishm,2,Torpedo Sting Ray,1,Torpedos,46,Torpedos MK 48,2,Torpedos MK 50,1,Toryu (SS-512),2,TR-1700,2,TR1700,5,Tracker,1,tragedia,2,Tramontana,1,Transferencia de Conocimiento,1,Transferencia de Tecnología,3,Transporte de submarinos,1,Triatlon,1,Trident,3,Trident II D5,1,Tripulacion.,1,Tripulaciones.,3,TTC Ayelén Gagliolo,1,TTC Marina Roberto.,5,Tubos Lanzatorpedos,5,TUP,1,Turkiye,41,Turquía,1,Type 094 SSBN,1,Type XXI,2,Type-039C,1,Type-212CD,15,U-10 S189,1,U-156,1,U-17 S-196,6,U-210,1,U-212 NFS,1,U-25,1,U-250,1,U-307,1,U-31,1,U-32,2,U-33,1,U-34,1,U-35,6,U-36,3,U-455,1,U-47,1,U-530,8,U-537,1,U-576,1,U-581,1,U-65,1,U-670,1,U-87,1,U-9,1,U-977,8,U-Boat,16,U-boats en Latinoamerica,10,U.S. Naval War College,1,U.S. Navy,1,U1 - Zaporiyia,2,U206,3,U206A,1,U212,22,U212 NFS,4,U212 NFS Todaro Class Batch-III,5,U214,1,U216,1,U35,1,U36,4,UBoat,46,UC-71,1,Ucrania,5,UDT,1,UET-1 ICTIONARIUS,1,UFEM,2,UMS Minye Theinkhathu,1,UNDEF,2,Undersea Defence Technology (UDT),1,Undersea Defence Technology Forum,1,Uniformes,1,Union Europea,2,Unión Soviética,1,Unitas,7,UNITAS LXVI,1,UPCT,1,URSS,19,US Naval Forces Southern Command & US 4th Fleet,1,US Navy,34,USMC,1,USNavy,309,USNI,1,USS Baton Rouge (SSN-689),2,USS Alabama (SSBN 731),1,USS Alaska,1,USS Albacore,1,USS Albacore (SS 218),1,USS Arkansas (SSN-800),1,USS Barb SSN 804,1,USS Batfish (SS-310),1,USS Boise,1,USS Bonefish,1,USS Bonefish SS-582,1,USS CATFISH (SS339),1,USS CHIVO (SS341),1,USS Clagamore (SS-343),1,USS Cobia,2,USS Colorado (SSN 788),1,USS Columbia (SSBN 826),1,USS Connecticut (SSN-22),7,USS CUBERA (SS-347),1,USS Delaware,1,USS Dogfish (SS350),1,USS Dolphin (AGSS-555),1,USS Frank Cable,1,USS Grayback (LPSS-574),1,USS Grayback (SS-208),1,USS GRENADIER (SS-525),1,USS GUARDFISH,1,USS Gurnard,1,USS Hampton (SSN-767),1,USS Harder (SS 257),1,USS Hawaii (SSN 776),4,USS Herring,1,USS Holland SS-1,1,USS Idaho (SSN-799),2,USS Illinois (SSN 786),2,USS Jacksonville (SSN 699),1,USS Jimmy Carter (SSN-23),1,USS La Jolla (SSN 701),1,USS Lamprey – (SS372),2,USS Ling,2,USS Ling
(SS-297),1,USS Louisiana (SSBN 743),1,USS Macabi (SS375),2,USS Massachusetts (SSN 798),3,USS MIAMI,2,USS Minnesota,1,USS Mississippi,1,USS Missouri,1,USS Montana SSN794,1,USS Montpelier,1,USS Nautilus (SSN-571),2,USS New Jersey,1,USS NEW JERSEY (SSN 796),2,USS New Mexico (SSN 779),2,USS O-5 (SS-66),1,uss ohio,1,USS Ohio (SSGN 726),2,USS Ohio (SSGN-726),1,USS Oklahoma City (SSN 723),1,USS Oregon (SSN 793),1,USS Pennsylvania (SSBN 735),1,USS S-4 (SS-109),1,USS San Francisco - (SSN-711),2,USS San Juan (751),1,USS Santa Fe,1,USS Scorpion (SSN-589),2,USS Sea Leopard (SS-483),1,USS Seawolf. (SSN 768),2,USS Skipjack,1,USS South Dakota,1,USS South Dakota (SSN-790),2,USS Spot (SS-413),1,USS Springer (SS-414),1,USS Springfield (SSN 761),1,USS Springfield (SSN-761),1,USS Squalus,1,USS STICKLEBACK (SS-415),1,USS Texas/SSN 775),1,USS Thornback (SS-418),1,USS Thresher,5,USS Tilefish (SS-307),3,USS Topeka (SSN 754),1,USS Trumpetfish (SS- 425),1,USS Utah,1,USS Vermont,1,USS Vermont (SSN 792),1,USS Washington (SSN 787),1,USS Wyoming,1,USS Wyoming (SSBN 742),1,UUV,11,UVV,4,V2,1,valdivia,1,Varshavyanka,1,vehículos aéreos no tripulados,1,Vehículos Submarinos Autónomos (AUV),1,vehículos submarinos no tripulados,18,Vehículos Submarinos no Tripulados (UUV),4,Veliki Nóvgorod,1,VERTREP,1,veteranos,1,Victoria Class,1,vida a bordo,46,Videos,40,Vietnam,14,Vigilancia y Reconocimiento),1,Vilit2021,1,Virginia Block VI,1,Visakhapatnam,1,Visitar un submarino,1,Visitas,7,Visitas a submarinos,2,Vistas a submarinos,4,VLS,1,VLS Sistemas de Lanzamiento Vertical,1,Volkhov,1,Walrus,8,Walter,1,Wartsila,1,Wass Submarine Systems,3,White Carillon,1,World Defence Show,1,worldofwarships,1,XLUUVS,3,Yasen,6,Yuan Class,1,Yuri Dolgoruki,2,Zapad2025,1,Zaporozhie,1,Zarpada,5,Zona de Hielo Marginal (MIZ),1,Zr.Ms. Dolfin,4,Zr.Ms. Dolphin,1,
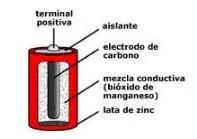 Las baterías, por medio de una reacción química producen, en su terminal negativo, una gran cantidad de electrones (que tienen carga negativa) y en su terminal positivo se produce una gran ausencia de electrones (lo que causa que este terminal sea de carga positiva). Ahora, si esta batería alimenta un circuito cualquiera, hará que por éste circule una corriente de electrones que saldrán del terminal negativo de la batería, (debido a que éstos se repelen entre si y repelen también a los electrones libres que hay en el conductor de cobre), y se dirijan al terminal positivo donde hay un carencia de electrones, pasando a través del circuito al que está conectado.
Las baterías, por medio de una reacción química producen, en su terminal negativo, una gran cantidad de electrones (que tienen carga negativa) y en su terminal positivo se produce una gran ausencia de electrones (lo que causa que este terminal sea de carga positiva). Ahora, si esta batería alimenta un circuito cualquiera, hará que por éste circule una corriente de electrones que saldrán del terminal negativo de la batería, (debido a que éstos se repelen entre si y repelen también a los electrones libres que hay en el conductor de cobre), y se dirijan al terminal positivo donde hay un carencia de electrones, pasando a través del circuito al que está conectado.







.jpg)








.jpg)







COMMENTARIOS